肺纤维化是由多种原因引起的肺间质的炎症性疾病,病变主要累及肺间质,也可累及肺泡上皮细胞及肺血管。 明确的病因有石棉、霉草尘、棉尘、药物及放射性损伤等等, 未知原因的称之为特发性肺纤维化 (IPF), 约占 65% 左右, 是一种特殊类型、慢性进展性、纤维化型间质性肺炎,主要发生于老年人,病变局限于肺部,组织病理学或(和)高分辨率 CT(HRCT)显示普通间质性肺炎(UIP)特征,平均生存时间仅 2-5 年 [1]。 目前药物治疗效果不佳,因此积极寻找有效靶点,一直是国内外研究的热点。 有大量临床及动物实验证明肺纤维化发病机制中存在氧化与抗氧化失衡[2]。 另外从2011年由 ATS、ERS、JRS 和 ALAT 共同制定的特发性肺纤维化诊治指南可以看出: 传统的激素及细胞毒药物强烈不建议使用,但是弱不推荐单用 N-乙酰半胱氨酸制剂。 Nrf2 (nuclea factor erythroid -2 -related factor 2)是一种氧化应激基本表达的关键转录因子,存在于全身多个器官,如肺脏、 肝脏、 肾脏、睾丸等,它的缺失或激活障碍直接引起细胞对应激源的敏感性变化。 通过激活 Nrf2/ARE 信号通路,可以增加抗氧化蛋白及Ⅱ相解毒酶的合成,进而人体增强的抗氧化能力, 达到延缓肺纤维化进展的目的。
1 Nrf2/ARE 传导通路组成
Nrf2/ARE 信号通路包括 3 个核心分子:Nrf2、 Kelch 样 ECH 相 关 蛋 白 l (Kelch -like ECHassociatedprotein 1,Keapl) 和抗氧化反应元件((antioxidant response element,ARE)[3]。
1.1 Nrf2 结 构 基 础 核 因 子 E2 相 关 因 子 2(Nuclearfactorerythroid-2p45-relatedfactor 2, Nrf2)属于 CNC 亮氨酸拉链转录激活因子家族,最早由 Moi 等 [4] 发现, 该家族有 6 个成员 p45 一Nfe2、Nrf1、Nrf2、Nrf3、BTB-CNC 异体同源体(Bachl)和 Bach2。 Nrf2 几乎在各种细胞内都可以表达,因此也被认为是成员中活性最强转录调节因子。有研究表明[5,6],Nrf1 在细胞组织分化、炎症及肿瘤等方面发挥重要功能。在不同种类的人和大鼠、鸡等的同源性分析发现的 Nrf2 基因含有 6 个结构域,分别被命名为(图 1)Nebl~6,其中 Neh1 即含有 CNC家族特有的 bZIP 结构域,bZIP 与小 Maf 蛋白(smallMafproteins)形成异二聚体,从而启动目标基因转录[7];Neh2 可与 Keapl 高度结合对 Nrf2 功能起负性调控作用 [8];Neh3 可维持 Nrf2 的转录活性[9];Neh4~5 同参与对 Nef2 目标基因转录活性的激活[10],Neh6 含有大量的丝氨酸残基,是非 Keap1 依赖的 Nrf2 降解的调控区域[11]。
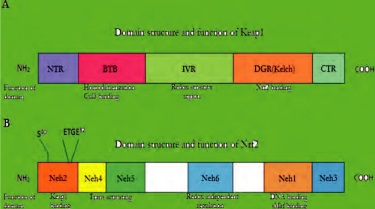
1.2 Keap1 结构基础 Keap1 因与果蝇肌动蛋白结合蛋白相似而被命名 Keapl 是一种含有 BTB 结构域的蛋白,主要包括 5 个结构域:N 末端序列 NTR (N-terminalregion);BTB 二聚化作用区域 (Broad - Complex Tramtrack,and Bric abrac), 是 Keap1 与 Cul3 作用的结构域,该结构域中的 C151 突变可使Keap1 与 Cul3 的作用解离, 进而导致 Nrf2 不被泛素化降解而积累; 含有 25 个半胱氨酸的 IVR(intervening region),可能是对亲电子化合物或氧化剂起反应的感应蛋白;DC 区域包括 6 个 Kelch 重复结构域 DGR(double glycine repeat) 和 C 端区域CTR(C-terminal region) 是与Nrf2-Neh2 相互作用的位点,也是与胞浆内肌动蛋白结合区位[11]。
1.3 ARE 结构基础 ARE 即抗氧化反应元件 ,是在编码谷胱甘肽巯基转移酶 Ya 启动子而发现的,其序列为 TGAnnnGC, 含有 1 个 API/TPA 反应元件即 TRE 元件 (TPA response element) 和 1 个类TRE 元件。 直至 Nrf2 基因被发现,人们对 ARE 的相关转录因子及结合蛋白逐渐了解, 对下游的抗氧化酶基因的表达具有重要作用, 其下游受其影响 的 基 因 主 要 包 括 NADH 苯 醌 氧 化 还 原 酶(NQOI)、 过氧化氢酶 (CAT)、 超氧化物歧化酶(SOD)、谷胱甘肽硫转移酶(GST)等。
2 Nrf2/ARE 传导通路活化机制
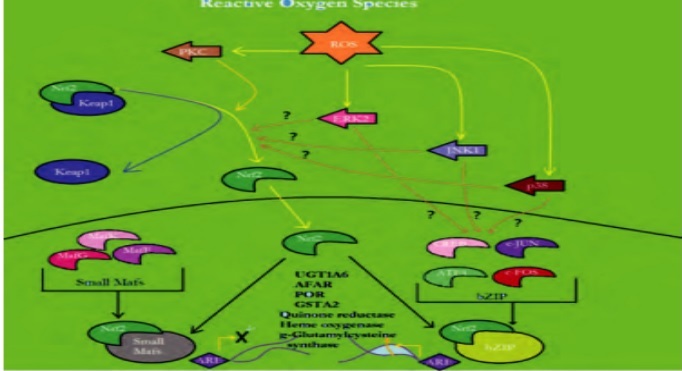
关于 Nrf2/ARE 的活化机制,最初认为是在正常生理情况下,Nrf2 通过与 Keapl 耦联, 并与肌动蛋白细胞骨架结合,同时被锚定于胞质,且稳定地存在细胞质中。 当氧化刺激、外源性化学物质或亲电子化合物的刺激下,半胱氨酸残基发生氧化,从而导致 Nrf2 和 Keapl 解耦联,Nrf2 从细胞质中易位至细胞核内,Nrf2 与其它的包括 Jun/Fos 家族、Fra、 小 Maf 和 ATF4 的 bZIP 蛋白形成异二聚体,与 ARE 相互作用, 从而激活抗氧化反应序列元件下游的Ⅱ相解毒酶基因及产生抗氧化酶的基因转录。 目前认为 Nrf2/ARE 通路主要由 MAPK(丝裂原活化的蛋白激酶),包含:ERK,JNK,P38、PKC(蛋白激酶 C)信号通路激活,具体机制有待进一步研究。其中包括谷胱甘肽转移酶(GST)、谷胱甘肽合成酶、谷氨酸半胱氨酸连接酶、过氧化氢酶、环氧化物水解酶、乙醛基转移酶、UGT 葡萄糖转移酶、醌氧化还原酶、 血红素加氧酶等众多解毒酶和抗氧化蛋白等细胞保护基因,这些基因的诱导表达,有助于增加细胞对氧化应激、 外源性化学物质及亲电子化合物刺激的抗性。
3 Nrf2/ARE 传导通路在肺部的表达
微阵列分析研究发现 Nrf2/ARE 通路可调节200 多种基因的表达, 这些基因主要编码解毒、抗氧化和谷胱甘肽生物合成酶等。 其中抗氧化酶有20 多种。 不同的器官 Nrf2 调控表达的基因数量和种类是不同, 由于肺脏具有独特的生理功能和解剖位置,直接与外界相通,并且持续暴露在较高的氧分压环境中,更易遭受氧化应激反应,因此 Nrf2/ ARE 通路在肺部主要调控抗氧化基因的表达 ,对肺组织起到保护作用。 这些基因有谷氨酰半胱氨酸连接酶 (glutamylcysteine ligase,GCL), 血红素加氧酶 1(haem oxygenase-1,HMOX1),γ-谷酰半胱氨酸合成酶 (γ-glutamyl cysteine synthetase,γ-GCS)等。
4 Nrf2/ARE 激动剂对氧化应激的抑制作用
大量的临床与实验研究表明, 肺纤维化的发生发展与氧化应激有着密切的关系,Nrf2/ARE 通路可以介导多种抗氧化酶及Ⅱ相解毒酶, 来保护人体组织,因此,Nrf2/ARE 通路诱导物有可能成为有潜力的基因靶向治疗药物。 我们在查阅文献时发现, 目前这一领域在呼吸系统疾病研究尚未开展,通过总结 Nrf2/ARE 通路激动剂对氧化应激导致病所发挥的治疗效果,可推测 Nrf2/ARE 的活化可能为肺纤维化的治疗带来新的方向。 目前,许多疾病化学预防剂已经进入临床实验, 包括莱菔硫(sulforaphane,SFN)、叔丁基对苯二酚(tBHQ)、丙炔苯丙胺、2-吲哚啉酮衍生物 PMID、齐墩果酸、苦参碱、 槲皮素等, 这些化合物都可以通过诱导 Nrf2/ ARE 下游基因的表达,保护细胞,减少氧化应激造成的损伤。 表 2 总结了氧化应激化学预防的疾病模型及表型。
5 展望
Nrf2/ARE 通路在肺内的保护和各项解毒酶的诱导表达中起关键作用, 可有效降低肺脏氧化应激的敏感性,目前国内外学者已经对 Nrf2/ARE 传导通路的作用机制进行了大量实验研究, 并且开展很多关于 Nrf2/ARE 通路激动剂的研究,取得明显效果。 但是,关于 Nrf2/ARE 信号通路对肺纤维化的调控仍然有许多问题亟需解答, 例如 ROS 作用于 Nrf2/ARE 通路的确切位点及作用机制、Nrf2/ARE 对 ROS 生成的反馈机制等等。 相信随着科学研究的深入,ROS 与 Nrf2/ARE 通路之间的相互作用机制一定会完整地展现在人们面前, 并在疾病的诊断和治疗中起重要的作用。
参考文献
[1]肖清萍,孙坚. 肺间质纤维化的发病机制研究进展[J]. 江西医药,2007,42(6):569-572.
[2]吴玉华 ,万乐乐. N-乙酰半胱氨酸治疗慢性阻塞性肺疾病合并肺间质纤维化疗效探讨[J]. 江西医药,2014,49(6):485-487.
[3]Moi P,Chan K,Asunis I,et al. Isolation of NF-E2-related factors 2(Nrf2),a NF -E2 -like basic leucine zippertranscriptional activator that binds to the tandem NF-E2/AP1 repeat of the h-globin locus control regions [J]. Procmurine AcadSci USA,1994,91 (21):9926 - 9930.
[4]Biswas M,Chan JY. Role of Nrfl in antioxidant response element-mediated gene expression and beyond [J]. Toxicol ApplPharmacol,2010. 244:16-20.
[5]Xu Z,Chen L,Leung L,et al. Liver-specific inactivation of the NIfl gene in adult mouse leads to nonalcoholicsteatohepatitis and hepatic neoplasia [J]. Proe Natl Acad Sci USA,2005,102:4120-4125.
[6]Radhakrishnan SK,Lee CS,Young P,et al. Transcription factor Nrf1 mediates the proteasome recovery pathway after proteasome inhibition in mammalian cells[J]. Mol Cell,2010,38:17-28.
[7]Takagi Y,Kobayashi M,Li L,et al. MafT,a new member of small Maf protein family in zebrafish[J]. Biochem Biophys Res Commun,2004,320:62-69.
[8]Zhang DD,Lo SC,Cross JV,et al. Keap1 is a redox -regulated substrate adaptor protein for a Cul3 -dependent ubiquitin ligase
[9]Nioi P,Nguyen T,Sherratt PJ,et al. The carboxy -termainal Neh3 domain of Nrf2 is required for transcriptional activation [J]. Mol Cell Biol,2005,25:10895-10906.
[10]Katoh Y,Itoh K,Yashida E,et al. Two domains of Nrf2 cooperati ̄ vely bind CBP,a CREB bingding preotein,and synergistically avtivate transcription[J]. Genes Cell,2001,6:857-868.
[11]McMahonM,ThomasN,Itoh K,et al. Redox -regulated turnover of Nrf2 isdetermined by at leasttwo separate protein domains,the redox-sensitive Neh2 degron and the redoxinsensitive Neh6 degron [J]. JBiol Chem,2004,279(30):31556-31567.
[12]Kobayashi M,ltoh K,Suzuki T,et al. ldentification of the interact ̄ ive interface and phylogenic conservation of the Nrf2 -Keap1 system[J]. Genes Cells,2002,7(8):807-820.
[13]Kang MI,Kobayashi A,Wakabayashi N,et al. Scaffolding of Keap1 to the actin cytoskeleton controls the function of Nrf2 as key regulator of cytoprotective phase 2 genes [J]. Proc Natl Acad Sci USA,2004,101(7):2046-2051
[14]Nguyen T,Sherratt PJ,Pickett CB. Regulatory mechanisms contro ̄ lling gene expression mediated by the antioxidant response element[J]. Annu Rev Pharmacol Toxicol,2003,43:233-260.
[15]Kim KC,Kang KA,Zhang R,et al. Up -regulation of Nrf2 - mediated heme oxygenase -1 expression by eckol,a phlorotannin compound,through activation of Erk and PI3K/Akt [J]. Int J Biochem Cell Biol,2010,42(2):297-305.
[16]朱运福,戴爱国,胡瑞成. 支气管哮喘豚鼠肺组织中 Nrf2 对 γ-GCS 的作用[J]. 中国应用生理学杂志,2006,22(4):493-495.
[17]张秀峰,戴爱国,胡瑞成. Nrf2 在支气管哮喘豚鼠炎症细胞中调γ-谷氨酰半胱氨酸合成酶的表达[J]. 中国病理生理杂志 ,2008,24(9):1779-1783.
[18]张凯茹 ,闫惠琴 ,王燕 ,等. Nrf2 及其靶基因在人肺腺癌 A549顺铂耐药细胞株中的表达和意义 [J]. 中国肺癌杂志,2009,12(11):1150-1154.
[19]倪静,秦丽娟,吴拥军,等. 肺癌组织中 Nrf2、Keap1 和 NQO1 蛋白的表达[J]. 郑州大学学报(医学版),2012,47(4):456-459.
[20]程风春,耿磊 ,李丽 ,等. 黄芩苷减轻大鼠肠缺血再灌注损伤及对 Nrf2、HO-1 表达[J]. 世界华人消化杂志,2014,22(11):1510-1517
[21]曹旭,肖海兵,杨燕,等. Nrf2 活化剂 SFP 对 MPP+所致 PC12 细胞氧化应激损伤的保护作用 [J]. 华中科技大学学报,2013,42(2):143-147.
[22]邢雁彬. 探讨百草枯中毒后 tBHQ 对肾脏氧化应激反应的影响[J]. 临床与实践,2013,17(31):4152-4153.
[23]李文娟. Nrf2 激动剂通过促进自噬对泛素化蛋白聚合物的清除保护氧化应激诱导胰岛 β 细胞损伤的作用及机制 [D]. 山东大学2014.
[24]冯健,何国祥 ,刘建平 ,等. 激动网织红核因子相关因子 2 对大鼠氧化应激所致血管平滑肌细胞损伤的影响[J]. 中华老年多器官疾病杂志,2013,12(3):226-229.
[25]Zhang T,Liang X,Shi L,et al. Estrogen Receptor and PI3K/Akt Signaling Pathway Involvement in S -(- )Equol -Induced Activation of Nrf2/ARE in Endothelial Cells[J]. PLOS ONE,2013,8(11):1-10.
[26]孔得刚 ,王莉莉 ,周洪雷. 樱桃汁和草莓汁激活 Nrf2 信号通路对砷诱导的人支气管上皮细胞损伤的保护作用[J]. 山东大学学报,2014,52(9):20-25.
[27]肖海兵. 丙炔苯丙胺对 MPP+诱导的帕金森病 PC12 细胞[D]. 华中科技大学,2011.
[28]秦方圆. 冬凌草甲素通过激活 Nrf2 通路保护肝细胞的研究[D].河南大学,2009.
[29]姚佳维. PMID 激活 Nrf2/ARE 信号通路的机制及其抗氧化作用研究[D]. 天津大学,2012.
[30]黄鹂. 丹酚酸 A 调控 Nrf2 通路对 HepG 细胞氧化损伤[D]. 大连医科大学,2011.
[31]赵春贞,王砚 ,唐法娣 ,等. 留兰香油对大鼠慢性阻塞性肺疾病模型肺组织炎症氧化改变和 Nrf2 蛋白表达的影响[J]. 浙江大学学报(医学版),2008,37(4):357-363.
[32]罗庆凯,何振华 ,张秀峰 ,等. 苦参碱对博莱霉素诱导的肺纤维化大鼠中 Nrf2 表达的影响[J]. 中国现代医学杂志,2012,22(13):16-20.
[33]申永春,杨婷 ,文富强 ,等. 槲皮素对香烟暴露大鼠肺组织氧化应激和 Nrf2 表达的影响[J]. 西部医学,2011,23(11):2071-2073.
|
