慢性阻塞性肺疾病( Chronic Obstructive Pulmonary Dis-ease,以下简称 COPD) 是一种以持续气流受限为特征的,可以预防和治疗的疾病,其气流受限多呈进行性发展,与气道和肺组织对烟草烟雾等有害气体或有害颗粒的慢性炎性反应增强有关[1]。近年来,有研究发现 COPD 等肺部慢性疾病的发生与发展中存在着不同程度的气道结构改变,这种气道结构的改变称为气道重塑。气道重塑可加重气道阻塞和气道高反应性,导致肺功能持续与进行性损害[2]。如何抑制气道重塑,减缓病情发展进程是治疗 COPD 的热点问题。本实验旨在通过测定 COPD 大鼠模型,通过测定大鼠气道壁厚度,探讨补益宗气法对 COPD 大鼠气道重塑的影响及机制。
1 材料
1.1 动物 纯系雄性 SD 大鼠( 购自南昌大学实验动物中心) ,分为正常对照组、模型组、治疗组,每组 10 只。
1.2 实验药品与主要试剂 补益宗气方: 生黄芪 30 g,西党参 30 g,炒白术 15 g,升麻 10 g,柴胡 10 g,陈皮 10 g,当归10 g,山萸肉 15 g,锁阳 15 g 等,由江西省中医院中药房提供煎煮,浓缩为含生药 1. 65 g /mL,低温保存于密封袋内;脂多糖( 美国 Sigma 公司产) ; 香烟( 每支焦油含量 13 mg,
尼古 1. 0 mg) 。
2 方法
2.1 造模 参照朱慧志等[3]的方法,第 1 d 和第 14 d,模型组及治疗组按 0. 2 mg /kg 量气管内注入脂多糖溶液。第2~ 13 d 及 15 ~ 28 d,模型组及治疗组每天在玻璃密闭箱,持续吸入点燃的香烟雾 30 min,所用香烟量约 20 支 /d,每次熏烟后立刻将大鼠移到室外( 室内外温差约 5 ℃ ) 冷风刺激 1 h,造模 28 d 结束。
2.2 给药 在造模的第 28d 开始给药直至第 42 d,模型组、治疗组分别予生理盐水及中药,剂量按体表面积折算率换算( S = K × W2 /3 S - 大鼠体表面积,K - 常数,取值 9.1, W- 大鼠体质量) [4]。
2.3标本制作 第 43 d 处死各组大鼠,取右肺下叶 10%甲醛固定,石蜡包埋切片,HE 染色及马松染色。
2.4 病理图象分析 随机对每只大鼠切片选取管壁内周长 < 1000um 的完整气道( 短长径比 > 0. 5) ,测量并计算: ① 管壁总面积( WAt) = 气道外壁所围面积( A0) - 管壁内侧面积( Ai) ; ②以管壁内周长( Pi) 进行标准化,结果表示为单位长度的管壁厚度( Wat /Pbm,μm2 / μm) ,即 Wat /Pbm =( A0 - Ai) /Pi[5]。
2.5统计学分析 SPSS 20. 0统计软件处理,数据以均数±标准差x ± s表示,组间采用q检验,以P < 0. 05为差异有显著性。
3 结果
3. 1 一般情况 正常对照组体形肥胖,强壮,皮毛光亮,活泼好动,呼吸平稳。模型组及治疗组均出现活动量减少,行动迟缓,躁动不安并且先后出现咳嗽、呼吸急促,毛发稀疏,竖毛,无光泽,食量减少,体质量下降等程度不一的情况。
3. 2病理形态学改变 在光镜下 HE 染色正常对照组小支气管未见腺体及炎性细胞浸润,黏膜纤毛柱状上皮细胞完整,纤毛排列整齐,肺泡壁完整肺泡结构正常连续,气道管壁无增厚。并可见模型组大鼠肺体积增大,表面苍白、粗糙不平。在光镜下马松染色可以观察到淋巴细胞等炎性细胞浸润,杯状细胞增生,支气管腔内中性粒细胞及黏液蓄积,气管黏膜下腺体增生肥大,支气管纤毛柱状上皮层增厚,皱褶高耸,平滑肌明显增厚,黏膜下及外膜胶原纤维增生,终末细支气管炎症明显,并且腔内常有中性粒细胞聚集,同时呼吸细支气管、肺泡、肺泡囊扩大,形成小叶中央性肺气肿。治疗组肺组织支气管壁及周围肺组织均见不同程度的嗜酸性粒细胞、淋巴细胞及浆细胞浸润,气道平滑肌的厚度较模型组薄,部分肺组织上皮结构残缺不齐,胶原纤维沉积程度不一,部分纤毛明显脱落,少量杯状细胞增生,肺泡扩张融合等,但不及 COPD 模型组明显,见插页Ⅱ图 1 ~ 图 2。
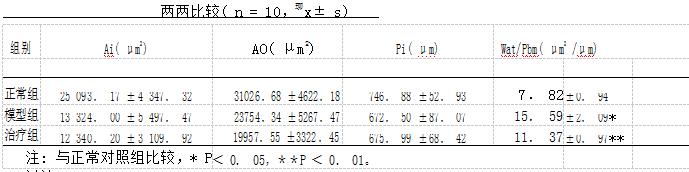
3. 3支气管管壁厚度测量 见表 1。从结果可以看出,模
型组大鼠所测气管壁厚于其他两组,且与正常对照组比较,差异有统计学意义( P < 0. 05) ,治疗组在给予补益宗气法干预后所测气道壁的厚度大于正常对照组水平 ( P <0. 01) ,但其气道增厚程度远不及模型组。由此可知补益宗气法可抑制 COPD 大鼠气道重塑。
表 1 各组大鼠管壁内侧平均面积( Ai) 、外壁所围平均面积( AO) 、管壁内平均周长( Pi) 平均值及管壁厚度
4 讨论
COPD 患者的发病与肺部对香烟、烟雾等有害气体或有害颗粒的异常炎症反应有关,患者支气管肺组织
中存在大量炎症细胞聚集、浸润,使气道壁受损,结构破坏。反复慢性炎症刺激损伤及不完全性修复逐渐导致支气管肺组织结构功能异常,也就是我们所说的气道重塑过程,表现为细胞外基质沉积增加、平滑肌增生肥大、气道壁增厚,上皮下层纤维化,黏液腺上皮化生等,最终导致管腔狭窄、肺气肿形成和进行性气流阻力增加[6]。本实验通过熏吸香烟、冷风刺激、气管内注入脂多糖的方法模拟多种 COPD 的发病因素,诱发大鼠气道炎症,在光镜下 HE 染色可以观察到炎性细胞浸润,气管黏膜下腺体增生肥大,支气管纤毛柱状上皮层增厚,平滑肌明显增厚,胶原纤维增生,肺泡壁破坏,形成小叶中央性肺气肿。说明造模成功。
COPD 属于中医“肺胀”、“喘证”等范畴,其病因病机复杂,目前普遍认为本病乃本虚标实之证。COPD 患者病程日久,久咳久喘,肺气虚衰,无力推动血行,则血行瘀滞,形成瘀血,痰瘀同阻于气道而致病,形成气虚痰瘀的证候特点。国医大师洪广祥教授根据该病这一证候特点以及其动则喘甚、肺病及心、呼吸肌疲劳、营养障碍等临床表现,认为宗气虚衰与 COPD 关系密切,提出从宗气论治 COPD,并取得较好的临床疗效[7]。
宗气是由经脾胃运化而来的水谷精气与经鼻从自然界吸入之清气相结合而成。医家张锡纯在《医学衷中参西录》指出宗气是“以元气为根本,以水谷之气为养料,以胸中之地为宅窟”,其作用是“贯心脉,行呼吸”,说明其有贯心脉以行营血和推动肺脏以行呼吸的作用。COPD 患者久咳久喘,肺气必虚,宗气生成不足,宗气是推动气血运行的根本动力,宗气虚衰,无力推动气血运行,气血瘀阻于心脉,瘀血内停,痰瘀互结,内伏于肺。宗气虚衰则肺脾之气化生无力,宗气缺乏物质基础而生成乏源,肺脾气虚,宗气生成不足,运化功能失司,津液内停成痰成饮,痰饮阻滞气道,气道壅塞,血行不畅,血滞为瘀。痰瘀互结,形成宿根,内伏于肺,进而形成气道阻塞的病理基础,这与现代学者对慢性阻塞性肺疾病气道重塑的认识是相一致的[8]。因此,通过补益宗气,可益气健脾补肺,助涤痰行瘀之功,以助达到补虚以祛实之目的。
本实验主要从补益宗气入手,方选洪广祥教授经验方补益宗气方,方中黄芪补中益气、升阳固表为君,配伍党参、甘草、白术补气健脾为臣,当归,养血和营,助党参、黄芪以补气养血,陈皮理气和胃,使诸药补而不滞,共为佐药,配以升麻、柴胡升阳举陷,协助君药升提下陷之中气,配以锁阳、山萸肉、熟附子,寓意补益宗气,益气举陷,固本培元。方中重用黄芪、西党参,以加强补益肺脾之气,并且,有研究表明,党参具有抗肿瘤、抗菌、抗氧化性、能增强免疫性,增强免疫细胞活性[9]等功效,而黄芪既能有效改善 COPD 患者的肺功能,又对气道炎症、气道重塑有一定的调节作用[10-11]。
目前西医对 COPD 多采用糖皮质激素与支气管舒张剂联合使用的方法治疗,范洪军[12]认为噻托溴铵联合舒利迭能够极大程度的改善患者肺功能,提高患者的生活质量及其存活率。余桂东[13]研究表明,糖皮质激素通过控制 IL -8、TNF - α 这一炎症因子,从未达到治疗目的。常规的西医治疗虽能改善症状,但很难阻断其病程进展,病人长期反复的慢性感染使机体的免疫功能下降,西医治疗在这时不仅会让病情加重,而且给患者带来沉重的经济负担。此时中医药对慢性阻塞性肺疾病的治疗显得尤为重要,并且中药治疗该病有明显的优势及独特之处[14]。本实验研究结果表明,补益宗气法,能抑制气道平滑肌的增生、肥厚,减轻气道重塑的程度,可能延缓慢性阻塞性肺疾病的病程进展,但仍对其具体作用机制还有待进一步研究。
参考文献
[1] 中华医学会呼吸病学分会慢性阻塞性肺疾病学组. 慢性阻塞性肺疾病诊治指南( 2013 年修订版) [S]. 中国医学前沿杂志 ( 电子版) ,2014,6( 2) : 67 - 80.
[2]苏琳,李娜. 慢性阻塞性肺疾病患者气道重塑及 T 淋巴细胞亚群与肺功能的相关分析[J]. 中华医院感染学杂志,2013, 23( 1) : 11 - 12.
[3]朱慧志,等. 多因素慢性阻塞性肺疾病大鼠模型的建立[J].中国临床保健杂志,2005,8( 2) : 145 - 146.
[4]赵伟,孙国志. 不同种实验动物间用药量换算[J]. 实验动物,2010,5: 52 - 53.
[5]金明哲,熊瑛. 沙美特罗替卡松粉吸入剂对大鼠慢性阻塞性肺疾病气道重塑的影响[J]. 医药导报,2014,33 ( 3) : 318 -322.
[6]崔德健. 加强对慢性阻塞性肺疾病气道重塑及其发生机制的研究,2004,9( 9) : 641 - 642.
[7]洪广祥. 补虚泻实法论治慢性阻塞性肺疾病[J]. 中医药通报,2006,5( 4) : 5 - 7.
[8]冯淬灵,武维屏. 络病理论与慢性阻塞性肺疾病气道重塑[J]. 北京中医药大学学报,2003,26( 4) : 75 - 76.
[9]陈克克,王品之. 党参多糖的研究进展田[J]. 现代生物医学进展,2007,7( 4) : 635 - 637.
[10]戴欢,张维溪. 黄芪在哮喘大鼠气道重塑模型中对 TGF -β1 /Smad3 信号通路的调控[J]. 中华中医药学刊,2010,12( 28) : 2494 - 2498.
[11]李慧,徐效峰. 黄芪对慢性阻塞性肺疾病疗效的 Meta 分析[J]. 中国全科医学,2013,16( 3A) : 805 - 807.
[12] 范洪军,顾宗玉. LAMA、ICS /LABA 在基层重度、极重度慢性阻塞性肺疾病稳定期的临床应用[J]. 中国现代药物应用,2014,8( 3) : 110 - 111.
[13]余桂东. 糖皮质激素对慢性阻塞性肺疾病患者 TNF - α 及IL - 8 的作用[J]. 实用医学杂志,2014,30( 2) : 330 - 331.
[14] 高峰,吴蔚,王彬,等. 中药干预对慢性阻塞性肺疾病稳定期患者临床疗效及生活质量的影响[J]. 中国中医药信息杂志,2012,19( 10) : 8 - 10.
|
